TỔNG QUAN ACETONE
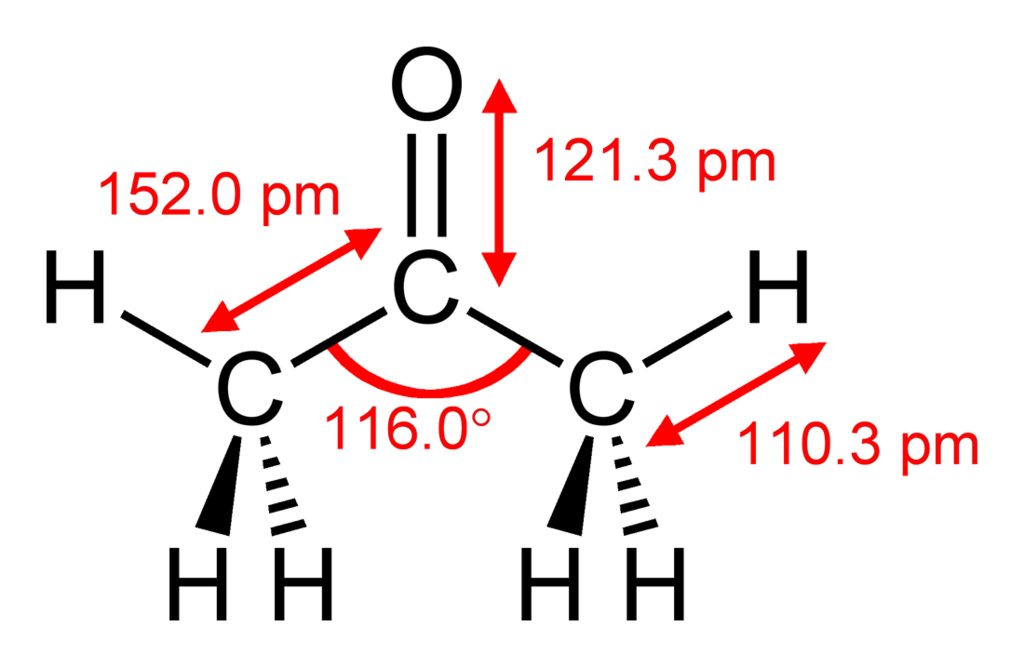
Acetone(tên hệ thống propanone) là hợp chất hữu cơ với công thức (CH 3 ) 2 CO. Đó là một không màu, dễ bay hơi, chất lỏng dễ cháy, và là đơn giản nhất xeton .
ACETONE
----oo0oo----
|
Acetone là có thể trộn với nước và phục vụ như một quan trọng dung môi theo đúng nghĩa của nó, thường để làm sạch các mục đích trong phòng thí nghiệm. Về 6,7 triệu tấn được sản xuất trên toàn thế giới trong năm 2010, chủ yếu là để sử dụng như một dung môi và sản xuất methyl methacrylate và bisphenol A. Đó là một khối xây dựng thông thường trong hóa học hữu cơ . Sử dụng trong gia đình quen thuộc của acetone như các thành phần tích cực trong việc tẩy sơn móng tay , và như sơn mỏng hơn. Acetone được sản xuất và xử lý trong cơ thể con người thông qua quá trình trao đổi chất bình thường. Nó là bình thường hiện diện trong máu và nước tiểu. Những người bị bệnh tiểu đường sản xuất ra nó với số lượng lớn hơn. Kiểm tra độc tính sinh sản cho thấy rằng nó có tiềm năng thấp gây ra vấn đề sinh sản. Phụ nữ mang thai, cho con bú và trẻ em có mức độ cao hơn của acetone. ketogenic chế độ ăn làm tăng acetone trong cơ thể được sử dụng để đối phó với động kinh cơn ở trẻ sơ sinh và trẻ em bị ngoan cố chịu nhiệt động kinh. Lịch sử Acetone lần đầu tiên được sản xuất bởi nhà giả kim thuật trong thời gian cuối thời Trung Cổ qua chưng cất khô axetat kim loại (ví dụ, chì axetat , mà sản xuất "tinh thần của sao Thổ" (kể từ khi biểu tượng giả kim chì cũng là biểu tượng chiêm tinh cho các hành tinh sao Thổ)). Năm 1832, nhà hóa học người Pháp Jean-Baptiste Dumas và hóa học người Đức Justus von Liebig xác định các công thức kinh nghiệm cho acetone. Năm 1833, nhà hóa học người Pháp Antoine Bussy tên acetone bằng cách thêm các hậu tố -one đến gốc của axit tương ứng (tức là, axit axetic ). Bằng năm 1852, nhà hóa học Anh Alexander William Williamson nhận ra rằng acetone là methyl acetyl ; năm sau, nhà hóa học người Pháp Charles Frédéric Gerhardt đồng tình. Năm 1865, nhà hóa học người Đức August Kekulé công bố công thức cấu trúc hiện đại cho acetone. Trong thời gian Thế chiến I, Chaim Weizmann phát triển quá trình phục vụ sản xuất công nghiệp của acetone (Weizmann Process).
Một lượng nhỏ acetone được sản xuất trong cơ thể bởi decarboxylation của cơ quan xeton . Một số mẫu chế độ ăn uống, bao gồm cả ăn chay kéo dài và chất béo cao thấp carbohydrate ăn kiêng, có thể sản xuất ketosis , trong đó axeton được hình thành trong mô cơ thể. Điều kiện sức khỏe nhất định, ví dụ như nghiện rượu và bệnh tiểu đường, có thể sản xuất nhiễm ceton acid , ketosis không kiểm soát được dẫn đến một sắc nét, và có khả năng gây tử vong, tăng nồng độ axit trong máu. Vì nó là một sản phẩm phụ của quá trình lên men, acetone là một sản phẩm phụ của ngành công nghiệp máy chưng cất.
Mặc dù một số sách giáo khoa hóa sinh và các ấn phẩm nghiên cứu hiện nay chỉ ra rằng acetone không thể được chuyển hóa, có bằng chứng ngược lại, một số có niên đại ba mươi năm. Acetone có thể được sản xuất từ quá trình oxy hóa của ăn isopropanol , hoặc từ tự phát / enzyme phân hủy của acetoacetate (một cơ thể xeton) ở những người ketotic. Nó sau đó có thể được chuyển hóa bằng cách CYP2E1 qua methylglyoxal để D -lactate và pyruvate , và cuối cùng là glucose / năng lượng, hoặc bằng một con đường khác nhau thông qua propylene glycol để pyruvate , lactate , acetate(có thể sử dụng cho năng lượng) và PROPANAL .
Trong năm 2010, năng lực sản xuất trên toàn thế giới cho acetone ước đạt 6,7 triệu tấn mỗi năm. Với 1,56 triệu tấn mỗi năm, Hoa Kỳ có khả năng cao nhất sản xuất, sau đó là Đài Loan và Trung Quốc đại lục . Các nhà sản xuất lớn nhất của acetone là INEOS Phenol , sở hữu 17% công suất của thế giới, với công suất cũng đáng kể (7-8%) bởi Mitsui , Sunoco và Shell vào năm 2010. INEOS Phenol cũng sở hữu địa điểm sản xuất lớn nhất thế giới (420.000 tấn / năm) trong Beveren (Bỉ). Giá giao ngay của acetone trong mùa hè 2011 là 1.100-1.250 USD / tấn tại Hoa Kỳ. Phương pháp hiện tại Acetone được sản xuất trực tiếp hoặc gián tiếp từ propylen . Khoảng 83% acetone được sản xuất thông qua quá trình CUMENE ; kết quả là, sản xuất acetone được gắn với sản xuất phenol. Trong quá trình CUMENE, benzen là alkyl hoá với propylen để sản xuất CUMENE , được oxy hóa bằng đường hàng không để tạo ra phenol và axeton: Quá trình khác liên quan đến quá trình oxy hóa trực tiếp propylene ( quy trình Wacker-Hoechst ), hoặc hydrat hóa của propylen để cung cấp cho 2-propanol , được ôxi hóa thành acetone. Phương pháp củ:
Trước đây, axeton được sản xuất bởi các phương pháp chưng cất khô của axetat , ví dụ canxi axetat trong decarboxylation ketonic . Ca(CH3COO)2 → CaO(s) + CO2(g) + (CH3)2CO (v) Sau thời điểm đó, trong thời gian Thế chiến thứ nhất , acetone được sản xuất bằng quá trình lên men acetone-butanol-ethanol với acetobutylicum Clostridium vi khuẩn , được phát triển bởi Chaim Weizmann (sau này là tổng thống đầu tiên của Israel ) để giúp các nỗ lực chiến tranh của Anh, trong việc chuẩn bị chất nổ không khói .lên men acetone-butanol-ethanol Điều này cuối cùng đã bị bỏ khi phương pháp mới với sản lượng tốt hơn đã được tìm thấy. Sửdung: Khoảng một phần ba của acetone trên thế giới được sử dụng như một dung môi, và một phần tư được tiêu thụ như cyanohydrin acetone , tiền thân của methyl methacrylate .
Acetone là một dung môi tốt cho nhiều loại nhựa và một số sợi tổng hợp. Nó được sử dụng cho mỏng polyester nhựa, dụng cụ sử dụng với nó dọn dẹp, và hòa tan gồm hai phần epoxy và superglue trước khi họ cứng. Nó được sử dụng như một trong những thành phần dễ bay hơi của một số loại sơn và vecni . Là một chất tẩy nhờn nặng, nó rất hữu ích trong việc chuẩn bị bằng kim loại trước khi sơn. Nó cũng hữu ích cho độ tin cậy cao hàn ứng dụng để loại bỏ nhựa thông sau khi hàn xong; điều này sẽ giúp ngăn chặn sự ảnh hưởng tia gỉ . Acetone được sử dụng như một dung môi của các ngành công nghiệp dược phẩm và như là một biến tính trong cồn biến tính .Acetone cũng có mặt như một tá dược trong một số dược phẩm . Mặc dù bản thân dễ cháy , axeton được sử dụng rộng rãi như một dung môi cho việc vận chuyển an toàn và lưu trữ của axetylen , mà không thể được an toàn áp lực như một hợp chất tinh khiết. Tàu có chứa một loại vật liệu xốp được làm đầy đầu tiên với acetone tiếp theo axetylen, mà tan vào axeton. Một lít acetone có thể hòa tan khoảng 250 lít axetylen ở áp suất 10 bar.
Acetone được sử dụng để tổng hợp methyl methacrylate . Nó bắt đầu với việc chuyển đổi ban đầu của acetone để acetone cyanohydrin : (CH3)2CO + HCN → (CH3)2C(OH)CN Trong bước tiếp theo, các nitrile được thủy phân để không bão hòa amide , được este hóa : (CH 3 ) 2 C (OH) CN + CH 3 OH → CH 2 = (CH 3 ) CCO 2 CH 3 + NH 3 Việc sử dụng thứ ba chính của acetone (khoảng 20%) được tổng hợp bisphenol A . Bisphenol A là một thành phần của nhiều polyme như nhựa polycarbonate , polyurethan , và nhựa epoxy . Quá trình tổng hợp liên quan đến việc ngưng tụ của axeton với phenol: (CH3)2CO + 2 C6H5OH → (CH3)2C(C6H4OH)2 + H2O Nhiều triệu kg acetone được tiêu thụ trong sản xuất dung môi methyl isobutyl alcohol và methyl isobutyl ketone . Những sản phẩm này phát sinh thông qua một ban đầu ngưng tụ nghịch đảo để cung cấp cho rượu diacetone . 2 (CH 3 ) 2 CO → (CH 3 ) 2 C (OH) CH 2 C (O) CH 3
Trong phòng thí nghiệm, axeton được sử dụng như một cực , dung môi không proton có trong một loạt các phản ứng hữu cơ , chẳng hạn như S N 2 phản ứng . Việc sử dụng acetone dung môi là rất quan trọng cho quá trình oxy hóa Jones . Nó không tạo thành một azeotrope với nước (xem azeotrope (dữ liệu) ). Đó là một dung môi phổ biến đối với rửa thủy tinh phòng thí nghiệm vì chi phí thấp và không ổn định. Mặc dù sử dụng chung của nó như là một lẽ đại lý làm khô , nó không phải là hiệu quả trừ bằng chuyển số lượng lớn và pha loãng. Acetone có thể được làm mát bằng đá khô để -78 ° C mà không đóng băng; acetone / phòng tắm đá khô thường được sử dụng để tiến hành phản ứng ở nhiệt độ thấp. Acetone là huỳnh quang dưới ánh sáng cực tím, và hơi của nó có thể được sử dụng như một tracer huỳnh quang trong các thí nghiệm dòng chảy.
Acetone được sử dụng trong một loạt các ứng dụng y tế và mỹ phẩm nói chung và cũng được liệt kê như là một thành phần trong các chất phụ gia thực phẩm và bao bì thực phẩm và cũng có trong tẩy sơn móng tay. Bác sĩ da liễu sử dụng acetone với rượu cho phương pháp điều trị mụn trứng cá để bóc da khô. Acetone thường được sử dụng trong lột hóa . Đại lý thường được sử dụng ngay hôm nay để mặt nạ hóa học là axit salicylic, axit glycolic , 30% axit salicylic trong ethanol , và axit tricloaxetic (TCA). Trước chemexfoliation, da được làm sạch và loại bỏ chất béo dư thừa trong một quá trình gọi là mất mỡ. Acetone, Septisol , hoặc sự kết hợp của các thuốc này thường được sử dụng trong quá trình này.
Acetone thường là thành phần chính trong chất tẩy rửa như sơn móng tay loại bỏ. Acetone là một thành phần của superglue loại bỏ và dễ dàng loại bỏ dư lượng từ thủy tinh và sứ. Make-up nghệ sĩ sử dụng acetone để loại bỏ chất kết dính da từ lưới của tóc giả và ria bằng cách dìm mục trong một bồn tắm acetone, sau đó loại bỏ các dư lượng keo làm mềm với một bàn chải cứng. Acetone cũng có thể được dùng kết hợp với chất lỏng hộp số tự động để tạo ra một loại dầu thâm nhập hiệu quả. Dầu phanh đôi khi được dùng ở vị trí của ATF. Những hỗn hợp (thường là 1: 1) có thể hữu ích trong việc nới lỏng bu lông gỉ hoặc bị mắc kẹt. Acetone thường được sử dụng cho đánh bóng hơi các hiện vật in trên mô hình 3D-in in với nhựa ABS. Kỹ thuật, được gọi là hơi acetone tắm mịn, liên quan đến việc đặt các phần in trong một buồng kín chứa một lượng nhỏ acetone, và sưởi ấm khoảng 80 độ C trong 10 phút. Điều này tạo ra một hơi của acetone trong container. Các acetone ngưng tụ đồng đều trên tất cả các phần, làm cho bề mặt để làm mềm và hóa lỏng. Sức căng bề mặt sau đó làm mềm nhựa bán lỏng. Khi phần được lấy ra từ buồng, thành phần acetone bốc hơi để lại một phần thủy tinh, mịn miễn striation, khuôn mẫu, và các cạnh lớp có thể nhìn thấy, đặc điểm chung trong không gian 3D in phần không được điều trị. Thấp cấp acetone cũng thường được sử dụng trong môi trường phòng thí nghiệm học tập như một tác nhân rửa thủy tinh để loại bỏ cặn và chất rắn trước khi rửa thức. An toàn
Thuộc tính nguy hiểm nhất của acetone là dễ cháy cực của nó. Ở nhiệt độ lớn hơn acetone của độ chớp cháy của -20 ° C (-4 ° F), hỗn hợp không khí từ 2,5% và 12,8% acetone, theo thể tích, có thể nổ hoặc gây cháy đèn flash. Hơi có thể chạy dọc bề mặt các nguồn bắt lửa từ xa và đèn flash trở lại. Tĩnh xả cũng có thể đốt cháy hơi acetone, mặc dù acetone có một điểm đánh lửa năng lượng khởi đầu rất cao và do đó vô tình đánh lửa là hiếm. Thậm chí đổ hoặc phun acetone trên than đỏ rực sẽ không đốt cháy nó, do nồng độ cao của hơi và tác dụng làm mát bốc hơi của chất lỏng. Nó tự động đốt cháy ở 465 ° C (869 ° F). Nhiệt độ tự bốc cháy cũng là phụ thuộc vào thời gian phơi sáng, do đó tại một số xét nghiệm nó được trích dẫn khi 525 ° C. Ngoài ra, acetone công nghiệp có khả năng chứa một lượng nước nhỏ mà cũng ức chế đánh lửa.
Bài chi tiết: acetone peroxide Khi oxy hóa, axeton tạo acetone peroxide như một sản phẩm phụ, mà là một cao không ổn định , chính nổ cao hợp chất. Nó có thể được hình thành vô tình, ví dụ như khi thải hydrogen peroxide được đổ vào dung môi thải có chứa acetone. Do sự bất ổn của nó, nó hiếm khi được sử dụng, mặc dù tổng hợp hóa học đơn giản của nó.
Acetone đã được nghiên cứu rộng rãi và thường được công nhận là có độc tính cấp tính và mãn tính thấp nếu nuốt phải và / hoặc hít. Acetone hiện không được coi là một chất gây ung thư , một đột biến hóa học hoặc một mối quan tâm cho mãn tính độc thần kinh ảnh hưởng. Acetone có thể được tìm thấy như một thành phần trong một loạt các sản phẩm tiêu dùng khác nhau, từ mỹ phẩm đến thực phẩm chế biến và chưa qua chế biến. Acetone đã được đánh giá là một là an toàn thường được công nhận (GRAS) chất khi hiện diện trong nước giải khát, thực phẩm nướng, món tráng miệng, và bảo tồn ở các nồng độ khác nhau, 5-8 mg / L.
Acetone được cho là triển lãm duy nhất độc tính nhẹ trong sử dụng bình thường, và không có bằng chứng mạnh mẽ về ảnh hưởng sức khỏe mãn tính nếu biện pháp phòng ngừa cơ bản được tuân thủ. Ở nồng độ hơi rất cao, acetone là khó chịu và, giống như nhiều loại dung môi khác, có thể ức chế hệ thống thần kinh trung ương . Nó cũng là một chất kích thích nghiêm trọng khi tiếp xúc với mắt, và một tiềm năng khát vọng phổi rủi ro. Trong một trường hợp tài liệu, ăn phải một lượng đáng kể acetone dẫn đến nhiễm độc toàn thân, mặc dù bệnh nhân cuối cùng hoàn toàn bình phục. Một số nguồn tin ước tính LD cho tiêu hóa của con người tại 0,621 g / kg; LD 50 hít bởi những con chuột được cho là 23 g / m 3 , hơn 4 giờ đồng hồ. Acetone đã được chứng minh là có thuốc chống co giật ảnh hưởng trong các mô hình động vật của chứng động kinh , trong trường hợp không độc, khi dùng ở nồng độ millimolar. Người ta đã đưa ra giả thuyết rằng carbohydrate thấp cao mỡ ketogenic chế độ ăn uống sử dụng trên lâm sàng để kiểm soát động kinh kháng thuốc ở trẻ em hoạt động bằng cách nâng acetone trong não. EPA EPCRA Hủy niêm yết (1995). EPA loại bỏ acetone từ danh sách các "hóa chất độc hại" được duy trì theo Mục 313 của Kế hoạch Khẩn cấp và cộng đồng phải biết luật (EPCRA). Khi đưa ra quyết định đó, EPA tiến hành một cuộc xem xét mở rộng của dữ liệu độc tính có sẵn trên acetone và thấy rằng acetone "triển lãm độc tính cấp tính chỉ ở mức độ đáng kể quá phát hành và tiếp xúc với kết quả", và thêm rằng acetone "triển lãm độc tính thấp trong các nghiên cứu kinh niên". Genotoxicity . Acetone đã được thử nghiệm trong hơn hai chục in vitro và in thử nghiệm in vivo. Những nghiên cứu này chỉ ra rằng acetone là không genotoxic. Tính gây ung thư . EPA năm 1995 kết luận, "Hiện nay chưa có bằng chứng cho thấy một mối quan tâm đối với chất gây ung thư". (EPCRA Rà soát, được mô tả trong mục 3.3). Các nhà khoa học NTP đã khuyến cáo chống lại mãn tính thử nghiệm độc tính / gây ung thư của acetone bởi vì "các nghiên cứu prechronic chỉ chứng minh một phản ứng độc hại rất nhẹ ở liều rất cao ở loài gặm nhấm". Độc thần kinh và phát triển thần kinh. Tiềm năng độc thần kinh của cả acetone và isopropanol , tiền thân trao đổi chất của acetone, đã được nghiên cứu rộng rãi. Những nghiên cứu này chứng minh rằng mặc dù tiếp xúc với liều cao acetone có thể gây ảnh hưởng hệ thống thần kinh trung ương thoáng qua, acetone không phải là một neurotoxicant. Một nghiên cứu độc tính thần kinh phát triển phương châm đã được tiến hành với isopropanol, và không có tác dụng gây độc thần kinh phát triển được xác định, ngay cả ở liều cao nhất được thử nghiệm. (SIAR, tr. 1, 25, 31). Môi trường. Khi EPA miễn acetone từ quy định như một hợp chất hữu cơ dễ bay hơi (VOC) năm 1995, EPA nói rằng sự miễn trừ này sẽ "đóng góp vào việc đạt được một số mục tiêu về môi trường quan trọng và sẽ hỗ trợ các nỗ lực phòng chống ô nhiễm của EPA". 60 Fed. Reg. 31.634 (16 tháng 6 năm 1995). 60 Fed. Reg. 31.634 (16 tháng 6 năm 1995). EPA lưu ý rằng acetone có thể được sử dụng như là một thay thế cho một số hợp chất được liệt kê như ô nhiễm không khí nguy hiểm (HAP) trong phần 112 của Đạo luật không khí sạch .
Mặc dù acetone xảy ra một cách tự nhiên trong môi trường trong nhà máy, cây xanh, khí núi lửa, cháy rừng, và như là một sản phẩm của sự phân hủy của chất béo cơ thể, phần lớn các acetone thải vào môi trường có nguồn gốc công nghiệp. Acetone bay hơi nhanh chóng, thậm chí từ nước và đất. Khi trong khí quyển, nó có một 22 ngày chu kỳ bán rã và được phân hủy bởi ánh sáng tia cực tím thông qua sự quang (chủ yếu là thành metan và etan ) tiêu thụ bởi các vi sinh vật góp phần vào việc tản của acetone trong đất, động vật, hoặc kênh rạch. Các LD của acetone cho cá là 8,3 g / L nước (tương đương khoảng 1%) so với 96 giờ, và thời gian bán hủy môi trường trong nước là khoảng 1 đến 10 ngày. Acetone có thể gây rủi ro đáng kể của sự suy giảm oxy trong các hệ thống thủy do sự tiêu thụ của vi sinh vật. |
Mời bạn tham khảo thêm tin tức mới tại địa chỉ : www.tpc.net.vn




 1
1
 2
2
 3
3